Het jaar opent met het vervolg op de hernieuwde toelating van de gentech anjer Moonaqua tm. Alle info tot nu toe.
EU vraagt uw mening over een gentech mais bestand tegen giffen.
Open Consultations
Maize Bt11 x MIR162 x MIR604 x 1507 x 5307 x GA21 EFSA Scientific Opinion on the assessment of genetically modified maize Bt11 x MIR162 x MIR604 x 1507 x 5307 x GA21 and subcombinations, for food and feed uses.
- EFSA opinion: 5 April 2019
- Deadline: 7 May 2019
- Make comments
Onze bezwaren van 17 april 2019.
Aanvullingen en verbeterde links, die niet meer bleken te werken van 19 april 2019.
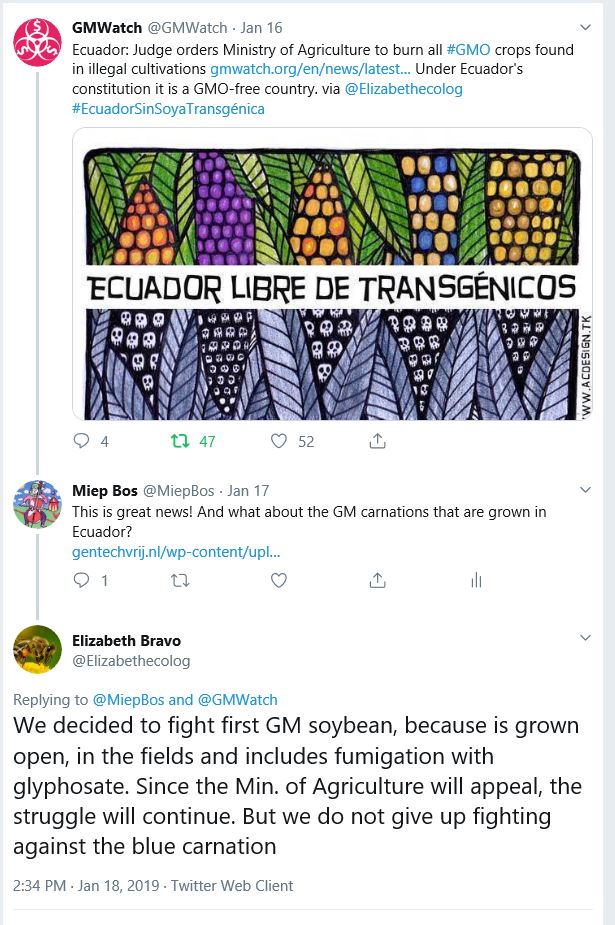
Ecuador is een Gentechvrije Zone
De rechter in Ecuador heeft het ministerie daar verzocht alle gentech gewassen te verbranden die illegaal worden verbouwd. Ecuador is namelijk een gentechvrij land. Omdat dat ministerie nog in beroep kan, richt men zich eerst op gentech soja die illegaal is aangeplant en waarbij Roundup wordt gespoten. Maar de strijd tegen de gentech anjer die daar in kassen wordt gekweekt gaat ook door. Dit schreef Mevr. E. Bravo ons via Twitter.
Op 10 januari 2019 stuurden we een antwoord op een brief van 21 december 2018 (net voor de Kerst!) aan de Juridische afdeling van I en W met een aantal verzoeken om machtigingen en uitleg over Stichting Ekopark en De Gentechvrije Burgers. We mochten er 4 weken over doen. We verzoeken in die aangetekende brief om telefonisch gehoord te worden. Vandaag 26 januari 2019 nog steeds geen datum ontvangen voor een telefonische hoorzitting. Intussen data genoemd. De eerste datum ging onverwachts op het laatste moment niet door een tweede datum op 21 maart 2019 wel. Lees de
Pleitnota en commentaar daarop behandeld tijdens de hoorzitting.


Beschikkingen die in 2019 afkwamen:
1.1 De Staatssecretaris van Infrastructuur en Waterstaat (hierna: de Staatssecretaris) heeft op 16 mei 2018 een aanvraag, gedateerd 14 mei 2018, van het Universitair Medisch Centrum Groningen te Groningen ontvangen. Deze aanvraag heeft het kenmerk IM-MV 18-003.
1.2 Het gaat om een aanvraag om een vergunning voor doelbewuste introductie voor overige doeleinden, als bedoeld in artikel 3.7, eerste lid, van het Besluit genetisch gemodificeerde organismen milieubeheer 2013 (hierna: Besluit ggo). De aanvraag heeft betrekking op een klinische studie in patiënten met glycogen storage disease type Ia (GSDIa). GSDIa is een ernstige, erfelijke, metabole ziekte. GSDIa wordt veroorzaakt door mutaties in het G6PC gen, dat codeert voor glucose-6-phosphatase-α (G6Pase). G6Pase is een enzym dat voornamelijk in de lever en niercortex tot expressie komt en betrokken is bij het glucose metabolisme. Patiënten met GSDIa hebben hypoglykemie en kunnen ernstige complicaties krijgen indien de ziekte niet wordt behandeld. De huidige behandeling van strikt dieet of levertransplantatie is echter niet toereikend.
Wij schreven een (verbeterde) zienswijze. Zie ook de Beschikking.
1.1 De Staatssecretaris van Infrastructuur en Waterstaat (hierna: de Staatssecretaris) heeft op 20 juni 2018 een aanvraag, gedateerd 18 juni 2018, van het Universitair Medisch Centrum Utrecht te Utrecht ontvangen. Deze aanvraag heeft het kenmerk IM-MV 18-009.
1.2 Het gaat om een aanvraag om een vergunning voor doelbewuste introductie voor overige doeleinden, als bedoeld in artikel 3.7, eerste lid, van het Besluit genetisch gemodificeerde organismen milieubeheer 2013 (hierna: Besluit ggo). De aanvraag heeft betrekking op klinische studies waarin autologe T-cellen van patiënten met maligniteiten, die B cell maturation antigen (BCMA) tot expressie brengen, ex vivo getransduceerd (genetische modificatie) worden met een lentivirale vector. Deze vector brengt een transmembrane, chimere anti-BCMA receptor (anti-BCMA CAR) tot expressie. De getransduceerde T-cellen worden weer teruggegeven aan de patiënten met als doel het induceren van een afweerreactie tegen deze maligniteiten.
Wij schreven een zienswijze. Zie ook de Beschikking.
1.1 De Staatssecretaris van Infrastructuur en Waterstaat (hierna: de Staatssecretaris) heeft op 4 juli 2018 een aanvraag, gedateerd 28 juni 2018, van het Prinses Máxima Centrum voor Kinderoncologie B.V., te Utrecht ontvangen. Deze aanvraag heeft het kenmerk IM-MV 18-010.
1.2 Het gaat om een aanvraag om een vergunning voor doelbewuste introductie voor overige doeleinden, als bedoeld in artikel 3.7, eerste lid, van het Besluit genetisch gemodificeerde organismen milieubeheer 2013 (hierna: Besluit ggo). De aanvraag heeft betrekking op klinische studies waarin autologe T-cellen van patiënten met B-cel tumoren ex vivo getransduceerd (genetische modificatie) worden met een lentivirale vector welke een transmembrane, chimere anti-CD19 receptor (anti-CD19 CAR) tot expressie brengt. De getransduceerde T-cellen worden weer teruggegeven aan de patiënten met als doel het induceren van een afweerreactie tegen de B-cel tumoren.
Wij schreven een (verbeterde) zienswijze. Zie ook de Beschikking.
1.1 De Staatssecretaris van Infrastructuur en Waterstaat (hierna: de Staatssecretaris) heeft op 14 september 2018 een aanvraag, gedateerd 12 september 2018, van het Academisch Ziekenhuis behorende bij de openbare universiteit Rotterdam te Rotterdam ontvangen. Deze aanvraag heeft het kenmerk IM-MV 18-015.
1.2 Het gaat om een aanvraag om een vergunning voor doelbewuste introductie voor overige doeleinden, als bedoeld in artikel 3.7, eerste lid, van het Besluit genetisch gemodificeerde organismen milieubeheer 2013 (hierna: Besluit ggo). De aanvraag heeft betrekking op een klinische studie in patiënten met Hemofilie A (bloederziekte). Hemofilie A is een ernstige, erfelijke bloedziekte veroorzaakt door een tekort aan functioneel factor VIII (FVIII). De ziekte treft ongeveer 1 op de 5.000 mannelijke pasgeborenen. Factor VIII is een eiwit dat noodzakelijk is voor bloedstolling. De ernst van de ziekte is afhankelijk van de resterende hoeveelheid FVIII die in de bloedbaan aanwezig is.
Wij schreven een zienswijze. Zie ook de Beschikking.
Wij geven nog wel commentaar op: Open Consultations
| Maize MON 89034 x 1507 x NK603 x DAS-40278-9 EFSA Scientific Opinion on the assessment of genetically modified maize MON 89034 x 1507 x NK603 x DAS-40278-9 and subcombinations independently of their origin, for food and feed uses. EFSA opinion: 16 January 2019 Deadline: 15 February 2019 Add your comments |
| Maize MON 89034 x 1507 x MON 88017 x 59122 x DAS-40278-9 EFSA Scientific Opinion on the assessment of genetically modified maize MON 89034 x 1507 x MON 88017 x 59122 x DAS-40278-9 and subcombinations independently of their origin, for food and feed uses under Regulation (EC) No 1829/2003 (application EFSA-GMO-NL-2013-113). EFSA opinion: 14 January 2019 Deadline: 13 February 2019 Add your comments |
| Soybean A2704-12 EFSA Scientific Opinion on the Assessment of genetically modified soybean A2704-12 for renewal of authorisation under Regulation (EC) No 1829/2003. EFSA opinion: 14 January 2019 Deadline: 13 February 2019 Add your comments |
| Maize MON 87427 × MON 89034 × MIR162 × NK603 Scientific opinion on application for authorisation of genetically modified maize MON 87427 × MON 89034 × MIR162 × NK603 and subcombinations for food and feed uses submitted under Regulation (EC) No 1829/2003 by Monsanto (EFSA- GMO-NL-2016-131) EFSA opinion: 8 July 2019 Deadline: 8 August 2019 Make comments |
| Soybean MON 87708 x MON 89788 x A5547-127 Scientific opinion on application for authorisation of genetically modified Soybean MON 87708 x MON 89788 x A5547-127 for food and feed uses submitted under Regulation (EC) No 1829/2003 by Monsanto (EFSA- GMO-NL-2016-135) EFSA opinion: 5 July 2019 Deadline: 8 August 2019 Make comments Bron EU. Meer over deze twee zie hier. |
In gelijk gesteld door EFSA, link was fout

We kregen samen met Christoph Then van Testbiotech vandaag een email van de EFSA dat onze klacht eindelijk is gehoord. Na veel emails naar steeds verkeerde invulformulieren, het bekende kastje naar de muur, kregen we eindelijk bericht dat er nu een goede link is naar een Scientific Opinion van de EFSA en dat de deadline is opgeschoven. Zie voor verdere details over de gentech 5 gestapelde maisaanvraag die via Nederland loopt, hier.
19 september 2019.
U kon reageren op een toelating van de gentech anjer (FLO-40685-2, Florigene® Moonvista™) tot de EU markt via Nederland
5 September is door de Minister van Infrastructuur en Waterstaat (hierna: IenW) vergunning verleend, met kenmerk GGO C/NL/13/02. De beschikking is op 16 september 2019 aan Suntory Holdings Limited verzonden.
Op 21 oktober 2013 had Suntory Holdings Limited een aanvraag ingediend.
Het zijn snijbloemen van een anjer met gewijzigde bloemkleur. (uit de bekendmaking.)
Alle info database GGO´s. Tweede kolom. Alles over onze petitie hierover en het bezwaar dat wij hebben verzonden.

Closed Consultations
We gave comments to all placings on the EU market in 2019. EU translated it into English.
Op alle markttoelatingen tot de EU markt in 2019 gaven we commentaar. De EU vertaalde de Nederlandse tekst in Engels. Wilt u de Nederlandse tekst lezen, stuur dan een e-mail.
| Soybean MON 87751 × MON 87701 × MON 87708 × MON 89788 Scientific opinion on application for authorisation of genetically modified Soybean MON 87751 × MON 87701 × MON 87708 × MON 89788 for food and feed uses submitted under Regulation (EC) No 1829/2003 by Monsanto (EFSA- GMO-NL-2016-128) EFSA opinion: 11 November 2019 Deadline: 11 December 2019 Comments received |
| Maize MON 89034 EFSA Scientific Opinion on the assessment of genetically modified maize MON 89034 for renewal authorisation under Regulation (EC) No 1829/2003 EFSA opinion: 7 November 2019 Deadline: 8 December 2019 Comments received |
| Maize MON 87427 x MON 89034 x MIR162 x MON 87411 EFSA Scientific Opinion on the Assessment of genetically modified maize MON 87427 x MON 89034 x MIR162 x MON 87411 and subcombinations, for food and feed uses, under Regulation (EC) No 1829/2003 EFSA opinion: 7 November 2019 Deadline: 8 December 2019 Comments received |
| Maize MIR604 EFSA Scientific Opinion on the assessment of genetically modified maize MIR604 for renewal authorisation under Regulation (EC) No 1829/2003 EFSA opinion: 7 November 2019 Deadline: 8 December 2019 Comments received |
| Maize 3272 EFSA statement complementing the EFSA Scientific Opinion on application for authorisation of food and feed containing, consisting of and produced from genetically modified maize 3272 EFSA complementing statement: 4 November 2019 EFSA opinion: 20 June 2013 Deadline: 4 December 2019 Comments received |
| Maize MON 87427 × MON 87460 × MON 89034 × MIR162 × NK603 Scientific Opinion on the assessment of genetically modified maize MON 87427 × MON 87460 × MON 89034 × MIR162 × NK603 and subcombinations for food and feed uses submitted under Regulation (EC) No 1829/2003 by Monsanto (EFSA- GMO-NL-2016-134) EFSA opinion: 8 August 2019 Deadline: 26 September 2019 Comments received Maize MON 87427 × MON 89034 × MIR162 × NK603 Scientific opinion on application for authorisation of genetically modified maize MON 87427 × MON 89034 × MIR162 × NK603 and subcombinations for food and feed uses submitted under Regulation (EC) No 1829/2003 by Monsanto (EFSA- GMO-NL-2016-131) EFSA opinion: 8 July 2019 Deadline: 8 August 2019 Comments received Soybean MON 87708 x MON 89788 x A5547-127 Scientific opinion on application for authorisation of genetically modified Soybean MON 87708 x MON 89788 x A5547-127 for food and feed uses submitted under Regulation (EC) No 1829/2003 by Monsanto (EFSA- GMO-NL-2016-135) EFSA opinion: 5 July 2019 Deadline: 8 August 2019 Comments received Maize Bt11 x MIR162 x MIR604 x 1507 x 5307 x GA21 EFSA Scientific Opinion on the assessment of genetically modified maize Bt11 x MIR162 x MIR604 x 1507 x 5307 x GA21 and subcombinations, for food and feed uses. EFSA opinion: 5 April 2019 Deadline: 7 May 2019 Comments received Oilseed rape T45 EFSA Scientific Opinion on the Assessment of genetically modified oilseed rape T45 for renewal of authorisation under Regulation (EC) No 1829/2003. EFSA opinion: 14 February 2019 Deadline: 14 March 2019 Comments received Maize MON 89034 x 1507 x NK603 x DAS-40278-9 EFSA Scientific Opinion on the assessment of genetically modified maize MON 89034 x 1507 x NK603 x DAS-40278-9 and subcombinations independently of their origin, for food and feed uses. EFSA opinion: 16 January 2019 Deadline: 15 February 2019 Comments received Maize MON 89034 x 1507 x MON 88017 x 59122 x DAS-40278-9 EFSA Scientific Opinion on the assessment of genetically modified maize MON 89034 x 1507 x MON 88017 x 59122 x DAS-40278-9 and subcombinations independently of their origin, for food and feed uses under Regulation (EC) No 1829/2003 (application EFSA-GMO-NL-2013-113). EFSA opinion: 14 January 2019 Deadline: 13 February 2019 Comments received Soybean A2704-12 EFSA Scientific Opinion on the Assessment of genetically modified soybean A2704-12 for renewal of authorisation under Regulation (EC) No 1829/2003. EFSA opinion: 14 January 2019 Deadline: 13 February 2019 Comments received |
Gentech blauwalgen
Kennisgeving Besluit genetisch gemodificeerde organismen milieubeheer 2013
Ontwerpbeschikking op de vergunningaanvraag van Photanol B.V. te Amsterdam, voor introductie in het milieu van genetisch gemodificeerde organismen
Vergunningaanvraag
Op 25 september 2019 heeft het Ministerie van Infrastructuur en Waterstaat (hierna: IenW) van Photanol B.V. te Amsterdam een vergunningaanvraag op grond van het Besluit genetisch gemodificeerde organismen milieubeheer 2013 (hierna: Besluit ggo) ontvangen voor introductie in het milieu van genetisch gemodificeerde organismen. De aanvraag is geregistreerd met het kenmerk GGO IM-L 19-001.
De aanvraag betreft werkzaamheden met genetisch gemodificeerde cyanobacteriën (algen) in een gesloten systeem. Door de genetische modificatie wordt beoogd een organisch zuur te produceren dat doorgaans op chemische wijze wordt verkregen. De aanvraag omvat cyanobacteriën (Synechocystis sp.) waarin enkele genen gericht zijn uitgeschakeld en genen zijn ingebracht die coderen voor een phosphatase en carboxylase die tezamen resulteren in productie van glycolzuur.
De werkzaamheden zijn voorgenomen plaats te vinden in de gemeente Delfzijl.
Op grond van het Besluit ggo dient de Minister van IenW op deze aanvraag te beslissen.
Procedure
Voor de behandeling van bovengenoemde aanvraag zal de uniforme openbare voorbereidingsprocedure worden doorlopen, conform afdeling 3.4 van de Algemene wet bestuursrecht.
17-12-2019: Ons bezwaar en dat van St. Ekopark.
———————————————————————————————————Hier stoppen onze zienswijzen, genoeg is genoeg. We hebben alles gezegd wat er gezegd kon worden sinds 1997 en er wordt niet geluisterd. Waar is het Nederlandse morele kompas gebleven? De enige onderwerpen waar we ons nu nog mee bezig gaan houden zijn de gentech anjers en EU consultations. En als het iets heel belangrijks betreft ook een bezwaar naar het Ministerie van I&W.



